
Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Tutkijat jäljittävät syöpää aiheuttavien solujen varhaisimmat fyysiset muutokset.
Viimeksi tarkistettu: 02.07.2025
 ">
">Kun syöpä diagnosoidaan, solu- ja molekyylitasolla on jo tapahtunut monia tapahtumia, jotka ovat jääneet huomaamatta. Vaikka syöpä luokitellaan kliinisissä tarkoituksissa varhais- ja myöhäisvaiheisiin, jopa "varhaisvaiheen" kasvain on seurausta monista aiemmista kehon muutoksista, jotka olivat havaitsemattomia.
Yalen yliopiston lääketieteellisen tiedekunnan (YSM) tutkijat ja heidän kollegansa ovat nyt saaneet yksityiskohtaisen käsityksen joistakin näistä varhaisista muutoksista käyttämällä tehokasta korkean resoluution mikroskopiaa seuratakseen ensimmäisiä syöpää aiheuttavia fyysisiä muutoksia hiiren ihosoluissa.
Tutkimalla hiiriä, joilla oli karvatuppien syöpää edistävä mutaatio, tutkijat havaitsivat, että syövän muodostumisen ensimmäiset merkit ilmenevät tiettyyn aikaan ja paikkaan hiirten karvatuppien kasvussa. Lisäksi he havaitsivat, että näitä syöpää edeltäviä muutoksia voidaan estää MEK-estäjiksi kutsutuilla lääkkeillä.
Tiimiä johti Tianchi Xin, PhD, tutkija YSM:n genetiikan laitoksella, ja siihen kuuluivat Valentina Greco, PhD, genetiikan professori YSM:ssä ja Yalen syöpäkeskuksen ja Yalen kantasolukeskuksen jäsen, sekä Sergi Regot, PhD, molekyylibiologian ja genetiikan apulaisprofessori Johns Hopkinsin lääketieteellisessä tiedekunnassa.
Heidän tutkimustulokset julkaistiin Nature Cell Biology -lehdessä.
Tutkijat tutkivat hiiriä, joille kehittyy ihon levyepiteelikarsinooma, toiseksi yleisin ihosyöpätyyppi ihmisillä. Näitä hiiriä muunneltiin geneettisesti lisäämällä niihin syöpää edistävä mutaatio KRAS-geenissä, joka on yksi yleisimmin mutatoituneista onkogeeneistä ihmisen syövissä. KRAS-mutaatioita on löydetty myös keuhko-, haima- ja paksusuolensyövistä.
Tutkijoiden tutkimiin varhaisiin muutoksiin kuului pienen, epänormaalin kyhmyn kasvu hiustupessa, joka luokitellaan syöpää edeltäväksi poikkeavuudeksi. "Näiden varhaisten tapahtumien ymmärtäminen voi auttaa meitä kehittämään lähestymistapoja syövän muodostumisen estämiseksi", sanoi tutkimuksen ensimmäinen kirjoittaja Xin.
Vaikka heidän tutkimuksensa keskittyy ihosyöpään, tutkijat uskovat, että heidän löytämiään periaatteita voitaisiin soveltaa moniin muihin KRAS-mutaatioiden aiheuttamiin syöpiin, koska näihin prosesseihin liittyvät keskeiset geenit ja proteiinit ovat samat kaikissa kasvaimissa.
Enemmän kuin vain solujen lisääntymistä Sekä ihmisillä että hiirillä karvatupet kasvavat jatkuvasti, karistavat vanhoja hiuksia ja muodostavat uusia. Kantasoluilla, joilla on kyky kehittyä erilaisiksi solutyypeiksi, on suuri rooli tässä uudistumisprosessissa. Aiemmat tutkimukset ovat osoittaneet, että KRAS-mutaatiot johtavat lisääntyneeseen kantasolujen lisääntymiseen karvatupissa, ja tämän kantasolujen suuren lisääntymisen ajateltiin olevan vastuussa syöpää edeltävästä kudossairaudesta.
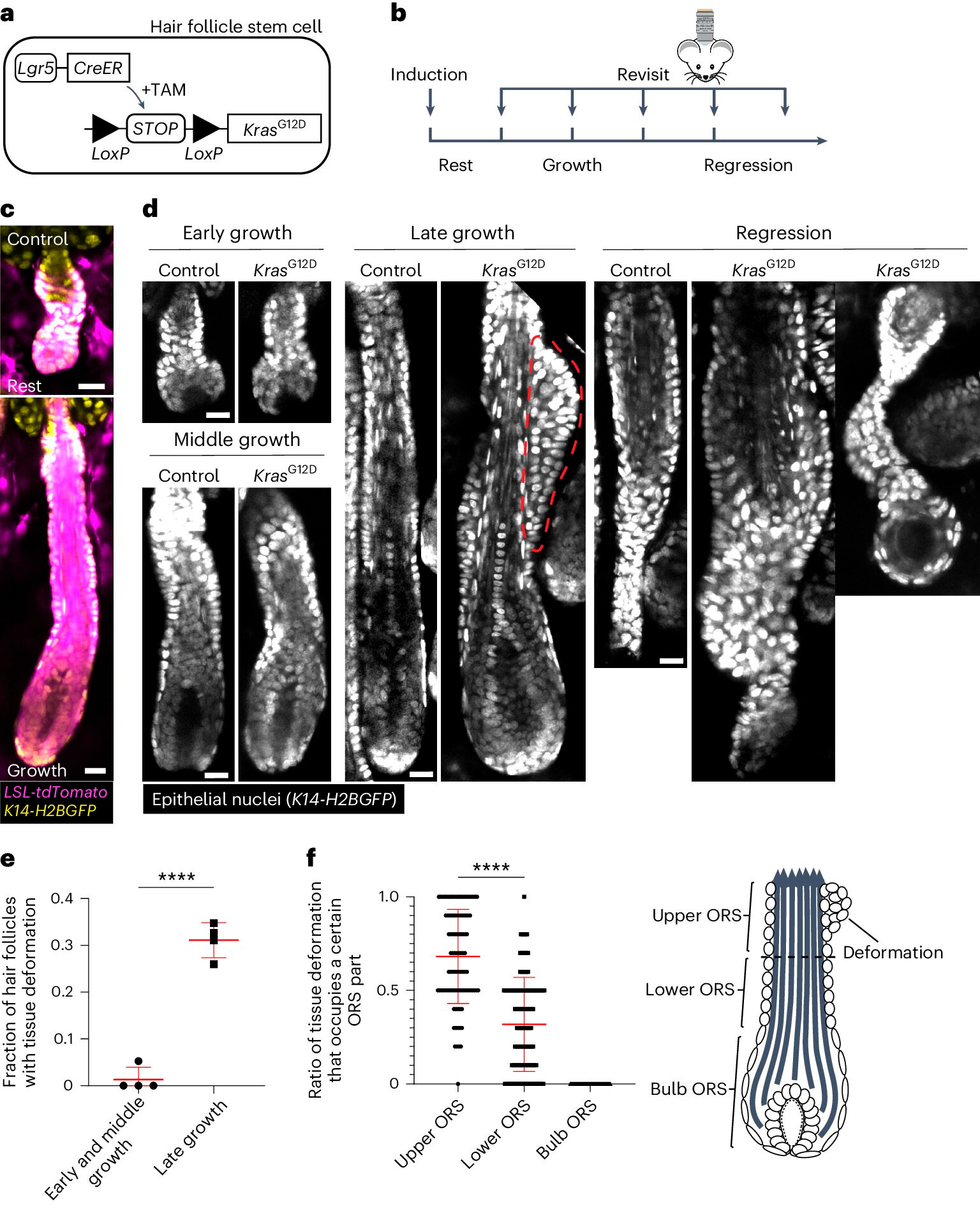
KrasG12D indusoi spatiotemporaalisia spesifisiä kudosmuodonmuutoksia hiusnystyn uudistumisen aikana.
A. Kaaviokuva geneettisestä lähestymistavasta KrasG12D:n indusoimiseksi hiusnystyn kantasoluissa käyttäen tamoksifeenilla indusoitavaa Cre-LoxP (TAM) -järjestelmää.
B. Kaaviokuva, joka esittää KrasG12D:n induktion ja uudelleenkuvantamisen ajoituksen suhteessa hiussyklin vaiheisiin.
C. Edustavat kuvat villityypin lepotilassa olevista ja kasvavista hiusnystynistä, jotka sisältävät Cre-indusoitavan tdTomato (Magenta) -reportterin induktion jälkeen.
D. Edustavat kuvat kontrolli- ja KrasG12D-hiusnystynistä eri hiussyklin vaiheissa. Kudosmuodonmuutos tuberkuloina ulommassa juuritupessa (ORS) on merkitty punaisella katkoviivalla.
E. KrasG12D-hiusnystyn osuus, jossa on kudosmuodonmuutoksia, hiusnystyn kasvun eri vaiheissa.
F. Yksittäisten KrasG12D-hiusnystyn ORS:n ylä-, ala- ja sipulimaisissa osissa olevien kudosmuodonmuutosten osuus.
Lähde: Nature Cell Biology (2024). DOI: 10.1038/s41556-024-01413-y
Tämän idean testaamiseksi tiimi käytti erityisesti suunniteltua mutatoituneen KRAS-geenin muotoa, jonka he pystyivät aktivoimaan tiettyinä aikoina eläinten karvatuppien ihosoluissa. Xin ja hänen kollegansa käyttivät mikroskopiatekniikkaa, joka tunnetaan nimellä intravitaalinen kuvantaminen, jonka avulla soluista voidaan ottaa korkearesoluutioisia kuvia in vivo ja merkitä ja seurata yksittäisiä kantasoluja eläimissä.
Kun KRAS-mutaatio aktivoitui, kaikki kantasolut alkoivat lisääntyä nopeammin, mutta syöpää edeltävä kyhmy muodostui vain yhteen tiettyyn kohtaan karvatupessa ja yhdessä kasvuvaiheessa, mikä tarkoittaa, että solujen määrän kokonaiskasvu ei todennäköisesti ollut koko totuus.
KRAS-mutaation aktivoituminen karvatupissa johti kantasolujen nopeampaan lisääntymiseen, niiden migraatiomallien muuttumiseen ja eri suuntiin jakautumiseen verrattuna soluihin, joissa ei ollut syöpää edistävää mutaatiota.
Mutaatio vaikuttaa ERK-nimiseen proteiiniin. Xin pystyi seuraamaan ERK:n aktiivisuutta reaaliajassa yksittäisissä kantasoluissa elävillä eläimillä ja havaitsi KRAS-mutaation aiheuttaman spesifisen muutoksen tämän proteiinin aktiivisuudessa. Tutkijat pystyivät myös pysäyttämään syöpää edeltävän kyhmyn muodostumisen käyttämällä MEK-estäjää, joka estää ERK:n aktiivisuutta.
Lääke pysäytti mutaation vaikutukset solujen migraatioon ja suuntautumiseen, mutta ei kantasolujen kokonaisproliferaatioon, mikä tarkoittaa, että syöpää edeltävän tilan muodostuminen johtuu näistä kahdesta ensimmäisestä muutoksesta eikä lisääntyneestä solujen lisääntymisestä.
Syöpää edeltävät muutokset kontekstissa Onkogeenisen mutaation vaikutusten seuraaminen reaaliajassa elävässä organismissa on ainoa tapa, jolla tutkijat ovat pystyneet paljastamaan nämä periaatteet. Tämä on tärkeää, koska syövät eivät muodostu tyhjiössä – ne ovat vahvasti riippuvaisia mikroympäristöstään kasvaakseen ja ylläpitääkseen itseään. Tutkijoiden piti myös seurata paitsi yksittäisten solujen käyttäytymistä myös näiden solujen sisällä olevien molekyylien toimintaa.
"Lähestymistapamme näiden onkogeenisten tapahtumien ymmärtämiseen perustuu pohjimmiltaan yhteyksien luomiseen eri tasoilla", Greco sanoi. "Tohtori Xinin ja tohtori Regotin käyttämä rakenne ja lähestymistavat ovat mahdollistaneet sen, että olemme voineet mennä molekyylitason elementteihin ja yhdistää ne solu- ja kudostasoon. Tämä on antanut meille ratkaisun näihin tapahtumiin, jota on niin vaikea saavuttaa elävän organismin ulkopuolella."
Tutkijat haluavat nyt seurata prosessia pidemmän ajanjakson ajan nähdäkseen, mitä tapahtuu alkuperäisen pullistuman muodostumisen jälkeen. He haluavat myös tutkia muita onkogeenisia tapahtumia, kuten tulehdusta, nähdäkseen, soveltuvatko heidän löytämänsä periaatteet muihin yhteyksiin.
