
Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Aivojen gliooma
Lääketieteen asiantuntija
Viimeksi tarkistettu: 29.06.2025
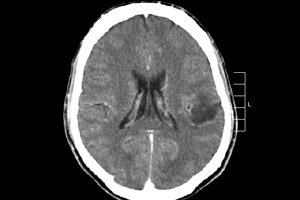
Keskushermoston monista kasvainprosesseista diagnosoidaan useimmin aivogliooma – tämä termi on kollektiivinen, kasvain yhdistää kaikki diffuusit oligodendrogliaaliset ja astrosyyttiset fokukset, astrosytooma, astroblastooma ja niin edelleen. Tällaisella kasvaimella voi olla eriasteista pahanlaatuisuutta, ja se muodostuu glia-rakenteista – hermosolujen ympärille paikantuneista soluista. Gliooman pääasiallinen sijaintialue on aivopuoliskot, aivokammioiden seinät ja kiasma – näköhermon kuitujen osittaisen leikkausalueen alue. Ulkoisesti kasvain on vaaleanpunainen tai punertava, pyöreä tai karanmuotoinen nodulaarinen elementti, jonka rajat ovat epäselvät. [ 1 ]
Epidemiologia
Noin 5 prosentissa tapauksista glioomiin liittyy perinnöllisiä sairauksia – erityisesti neurofibromatoosia ja muita vallitsevasti periytyviä oireyhtymiä. Asiantuntijat huomauttavat, että absoluuttinen enemmistö aivoglioomista kehittyy satunnaisesti – eli ilman selkeää syytä.
Keskushermoston primaariset kasvaimet muodostavat noin 2 % kaikista kasvaimista eli hieman yli 21 tapausta sataatuhatta asukasta kohden. Näistä glioomia esiintyy 35–36 %:ssa tapauksista, ja yli 15 % niistä on glioblastoomia.
Joidenkin tietojen mukaan gliooma vaikuttaa miehiin useammin kuin naisiin - kasvain on erityisen yleinen yli 50-vuotiailla.
Gliooman ilmaantuvuus ikääntyneillä on lisääntynyt merkittävästi viime vuosikymmeninä maailmanlaajuisesti. Tämän ilmiön syitä ei ole vielä selvitetty.
Maailman terveysjärjestön määritelmän mukaan on tunnistettu kolme pääasiallista gliakasvainten varianttia, jotka eroavat toisistaan histologisten ominaisuuksiensa suhteen. Nämä ovat oligodendroglioomat, astrosytoomat ja yhdistetyt oligoastrosytoomat. Kunkin lievän pahanlaatuisen patologian alatyypin esiintyvyyttä ei ole luotettavasti määritetty. Jotkut tutkimukset osoittavat oligodendroglioomien esiintyvyyden lisääntyneen 5 prosentista 30 prosenttiin ja astrosytoomien esiintyvyyden vähenevän.
Gliasolukasvaimet pystyvät tunkeutumaan aivokudokseen, ja valtaosa matala-asteisista kasvupesäkkeistä muuttuu pahanlaatuisiksi muutamassa vuodessa. [ 2 ]
Syyt aivojen glioomat
Aivogliooma on joukko kasvainprosesseja, joille on yhteistä niiden muodostuminen aivokudoksessa sijaitsevista keskushermoston glia-rakenteista. Tällaiset kasvaimet jaetaan kahteen histopatologiseen varianttiin: korkean pahanlaatuisuuden ja matalan pahanlaatuisuuden glioomiin.
Kasvun muodostumisen lähde on neurogliasolut (astrosyytit, oligodendrosyytit), jotka tarjoavat aivojen hermosolujen rakenteellisen perustan ja elinkelpoisuuden.
Gliasolujen kasvainprosessit eroavat suuresti toisistaan rakenteensa, geenien mutaatiomuutosten, aggressiivisuutensa, kliinisten piirteidensä, diagnostisten ominaisuuksiensa, hoitovasteensa ja potilaiden ennusteensa suhteen. Keskushermoston alkion- ja ependyymatuumorit - erityisesti medulloblastoomat ja ependymoomat - eroavat toisistaan histologisen rakenteensa suhteen, mutta ovat samankaltaisia hoidon suhteen.
Gliaelementit luokiteltiin ensimmäisen kerran erilliseksi hermoston rakenteelliseksi luokaksi 1800-luvun lopulla.
Neurogliakudos koostuu soluista, joilla on aputoimintoja: troofisia, tuki-, suojaavia ja erittäviä. Neuronit ja gliosyytit esiintyvät yhdessä, ne muodostavat yhdessä hermoston ja ovat erittäin tärkeitä organismin elintärkeän toiminnan yleisissä prosesseissa.
Gliosyytit luokitellaan karkeasti useisiin päätyyppeihin: astrosyytteihin, oligodendrosyytteihin, ependyymisoluihin ja mikrogliaan.
Tähän mennessä tiedemiehet eivät pysty vastaamaan kysymykseen neurogliakasvainten muodostumisen luotettavista syistä. Oletettavasti radioaktiiviset vaikutukset, tartuntataudit ja myrkytys (erityisesti kemiallinen, ammatillinen) vaikuttavat tiettyyn negatiiviseen vaikutukseen. Myös perinnöllisyydellä on merkitystä.
Aivoglioomat syntyvät epänormaaleista neurogliosyyteistä, joissa on geneettinen vika, joka johtaa epänormaaliin kasvuun ja toimintaan – tällaisia rakenteita kutsutaan "epäkypsiksi". Epätäydelliset solut sijaitsevat useammin yhdellä alueella, jossa kasvain muodostuu.
Yksinkertaisesti sanottuna gliasolujen muodostuminen on seurausta modifioitujen neurogliasolujen kaoottisesta ja satunnaisesta kasvusta. Prosessi voi kehittyä ependymosyyteistä, oligodendrosyyteistä, astrosyyteistä (astrosytooma, mukaan lukien jättisolu- ja anaplastiset taudit). [ 3 ]
Riskitekijät
Huolimatta siitä, että asiantuntijat eivät pysty tarkasti kuvaamaan glia-onkopatologioiden muodostumisen syitä, joissakin tapauksissa niiden ulkonäkö voidaan estää poistamalla tärkeimmät riskitekijät:
- Ionisoivalla säteilyllä on karsinogeenista vaikutusta, ja se voi aiheuttaa leukemian kehittymistä ja tiheän rakenteen omaavien syöpäprosessien muodostumista, myös nuorilla henkilöillä. Myös usein toistuvat ja kohtuuttomat radiologiset lääketieteelliset toimenpiteet ja ultraviolettisäteily (mukaan lukien solarium) ovat potentiaalisesti karsinogeenisia vaikutuksia ja voivat aiheuttaa kasvainten esiintymistä eri elimissä, mukaan lukien aivoissa.
- Työperäisillä haittavaikutuksilla, päihtymyksillä, on usein syy-yhteys syöpäkasvainten kehittymiseen. Kumin ja lasin, torjunta-aineiden ja polttoaineiden, metallien ja tekstiilien, maalien ja laboratorioreagenssien tuotantoa pidetään erityisen vaarallisena. Riskiryhmässä ovat ilmailu- ja avaruusteollisuuden, hiili- ja metalliteollisuuden, kemian- ja sivutuotetehtaiden, rakennusmateriaalien ja elektrodien, polttoaineiden ja voiteluaineiden, muovien ja monomeerien työntekijät.
- Ilman, veden ja maaperän saastuminen on vastuussa jopa 4 prosentista kaikista maailman syöpätapauksista. Ympäristössä suuria määriä esiintyviä karsinogeeneja pääsee elimistöön hengitettynä ilman, juomaveden ja ruoan mukana. Ekologisesti vaarallisilla alueilla – suurten teollisuuslaitosten ja vilkkaiden liikenneyhteyksien lähellä – asumista pidetään erityisen vaarallisena.
- Tartuntataudit - erityisesti virusinfektiot - voivat myös luoda suotuisat olosuhteet kasvainten kehittymiselle. On tärkeää pitää tämä mielessä ja rokottaa itsesi etukäteen sekä ehkäistä tartunta- ja loistauteja.
- Tupakka- ja alkoholipäihtymystä pidetään monien syöpätyyppien, ei vain aivoglioomien, riskitekijöinä.
- Riittämätön fyysinen aktiivisuus, ylipaino, epäterveellinen ravitsemus, aineenvaihduntahäiriöt, pään vammat, verisuonitaudit - lisästressitekijät, jotka voivat aiheuttaa solunsisäisten häiriöiden alkamista.
- Vanhempi ikä on yleisin ajanjakso kasvainten kehittymiselle kehossa, joten yli 55-vuotiaiden tulisi pitää erityistä huolta omasta terveydestään.
Tärkein ja merkittävin gliooman kehittymisen riskitekijä on kuitenkin edelleen perinnöllinen alttius.
Synnyssä
Tähän mennessä asiantuntijoilla on useita oletuksia aivoglioomien kehityksestä. Jokaisella teorialla on omat perusteensa, mutta ainoaa oikeaa ja luotettavaa patogeneettistä mekanismia tutkijat eivät ole vielä tunnistaneet. Useimmissa tapauksissa puhumme seuraavista tekijöistä kasvainten kehityksessä:
Alkionkehityksen epäonnistuminen, joka koostuu elinten muninnan häiriintymisestä ja "väärien" solurakenteiden muodostumisesta;
- Altistuminen ionisoiville säteille, mahdollisille karsinogeeneille kemiallisten aineiden muodossa, elintarvikelisäaineille jne.;
- Pään trauma;
- Sukupolvelta toiselle siirtyvät geenihäiriöt ("perinnöllinen" gliooma);
- Immuunijärjestelmän toimintahäiriöt, neuroinfektiot.
Useimmilla glioomilla on diffuusi kasvu, joka tunkeutuu ympäröivään normaaliin aivokudokseen. Kasvaimen pahanlaatuisuudesta riippuen se voi kehittyä useita vuosia ilman oireita. Aggressiivisessa taudinkulussa oireet lisääntyvät nopeasti useiden kuukausien aikana.
Osa kasvainten synnystä johtuu dysembryogeneettisistä muutoksista.
Aivorunko voi vaurioitua eri tasoilla: diffuusi aivorungon gliooma puolestaan eroaa sekä anatomis-morfologisesti että kliinisesti. Jotkut tällaiset kasvaimet – erityisesti neliraajahalvauslevyn gliooma – voivat olla suhteellisen hyvänlaatuisia ilman etenemisen merkkejä. Toisaalta pontiiniglioomalle on ominaista sen erityinen pahanlaatuisuus, aggressiivisuus ja huono ennuste.
Aivorakenteiden diffuusit leesiot, joissa patologiseen prosessiin osallistuu yli kolme aivopuoliskon anatomista vyöhykettä, ja joissa on mahdollista periventrikulaarista divergenssia ja kulkua korpuskutsussa gliomatoosina. [ 4 ]
Onko aivoglioma perinnöllinen?
Hyvin todistettu aivogliooman muodostumisen riski on perinnöllinen – eli samankaltaisten tai muiden aivokasvainten esiintyminen suorilla esi-isillä tai samassa sukupolvessa. Radioaktiivinen altistuminen ja säännöllinen tai pitkäaikainen kosketus mahdollisten karsinogeenien kanssa pahentavat tilannetta.
Glioomat voivat periä paitsi perinnöllisiä, myös sairauksia, joihin liittyy lisääntynyt kasvaimen kasvu sijainnista riippumatta - erityisesti tämä voi olla neurofibromatoosi tyypit 1 ja 2, Li-Fraumeni-oireyhtymä, Hippel-Lindau. Usein glioomasoluissa havaitaan muutoksia tietyissä geeneissä tai kromosomeissa.
Taulukossa on esitetty tärkeimmät gliooman kehittymiseen liittyvät patologiat ihmisillä:
Patologia |
Kromosomi |
Geeni |
Kasvainten monimuotoisuus |
Li-Fraumeni-oireyhtymä |
17.13. |
TR53 |
Neuroektodermaaliset kasvaimet, astrosytooma. |
Neurofibromatoosi |
17q11 |
NF1 |
Näköhermon gliooma, pilosyyttinen astrosytooma, neurofibromatoosi |
Turcotten oireyhtymä |
3p21, 7p22 |
HMLH1, HPSM2 |
Astrosytooma |
Tuberoosi skleroosi (Burnevillen oireyhtymä). |
9q34, 16p13 |
TSC1, TSC2 |
Gigantosellulaarinen subependymaalinen astrosytooma |
Gliasolukasvaimen luonteesta riippumatta, olipa kyseessä sitten satunnainen tapaus tai perinnöllinen patologia, se on häiriö, johon liittyy patologisesti muuttuneen geenin ilmentyminen. Oppimisvaikutusten seurauksena muodostuneita kasvaimia lukuun ottamatta muissa tilanteissa geneettisten muutosten syyt ovat edelleen epäselviä.
Oireet aivojen glioomat
Fokusoireiden ominaisuudet riippuvat suoraan aivogliooman lokalisointialueesta ja tulevat seuraukseksi kaikenlaisista hormonaalisista häiriöistä, hermokudoksen puristumisesta tai paikallisista tuhoisista prosesseista.
Jos kasvain sijaitsee parietaalivyöhykkeellä, henkilöä hallitsevat sellaiset ilmenemismuodot kuin kouristukset, aistihäiriöt ja kuulovamma.
Kun gliooma lokalisoituu hallitsevan aivopuoliskon alueelle, havaitaan puhehäiriöitä, agrafiaa, agnosiaa.
Ohimolohkon kasvaimiin liittyy usein kouristuskohtauksia, afasiaa, heikentynyt hajuaisti ja näkötoiminto sekä hengenahdistus.
Kun kallonsisäinen paine nousee, kehittyy vastaava kuva, johon liittyy näkökenttien supistuminen, silmälihasten halvaantuminen ja hemiplegia.
Kasvainprosessin spesifisyyden vuoksi aivoglioomaan liittyy aina enemmän tai vähemmän neurologisia oireita. Aluksi on havaittavissa yleinen heikkous, potilas haluaa jatkuvasti nukkua, työkyky on heikentynyt ja ajatusprosessit hidastuvat. Tässä vaiheessa on suuri riski tehdä väärä diagnoosi ja sen seurauksena määrätä väärä hoito. Muita epäspesifisiä ilmenemismuotoja ovat:
- Vestibulaariset häiriöt, mukaan lukien epävakaa kävely, tasapainon menetys (esim. pyöräillessä tai portaita kiivetessä), raajojen tunnottomuus jne.;
- Näön asteittainen heikkeneminen, visuaalisen kuvan kaksinkertaistuminen;
- Kuulotoiminnan heikkeneminen;
- Sokellus;
- Pahoinvointi ja oksentelu hyökkäysten muodossa, jotka eivät liity ruokaan tai juomaan;
- Näön ja muiden kasvolihasten heikkeneminen;
- Epämukavuus nielemisen aikana;
- Säännölliset päänsäryt (usein aamulla).
Kliininen kuva laajenee ja pahenee vähitellen: joillakin potilailla se tapahtuu hitaasti, toisilla - äkillisesti, kirjaimellisesti "heidän silmiensä edessä", muutaman viikon kuluessa. Jälkimmäisessä tapauksessa puhumme aggressiivisesta, nopeasti kehittyvästä aivojen glioomasta.
Ensimmäiset merkit
Aivojen gliooma varhaisessa kehitysvaiheessa ei ole selvä oireyhtymä. Ensimmäiset ilmenemismuodot sekoitetaan usein muiden, vähemmän vaarallisten patologioiden merkkeihin.
Yleisesti ottaen gliooman kliininen kuva on monipuolinen ja määräytyy patologisen pesäkkeen sijainnin ja koon mukaan. Kasvaimen kasvaessa yleiset aivo-oireet kehittyvät ja lisääntyvät:
- Jatkuva ja säännöllinen päänsärky, joka ei reagoi tavanomaisiin lääkkeisiin (ei-steroidiset tulehduskipulääkkeet);
- Ajoittainen pahoinvointi, joskus jopa oksenteluun asti;
- Epämiellyttävä, raskas tunne silmämunan alueella;
- Kouristukset.
Aivojen ilmentymät ovat erityisen voimakkaita, kun kasvain kasvaa kammioihin tai liquorijärjestelmään. Aivo-selkäydinnesteen tyhjennys on heikentynyt, kallonsisäinen paine nousee ja kehittyy vesipää. Prosessi vaikuttaa tiettyyn aivojen osaan, mikä vaikuttaa vastaavan klinikan kehitykseen:
- Näkötoiminnossa on ongelmia;
- Puhevamma;
- Vestibulaarisia häiriöitä (huimausta, liikkeiden koordinaation heikkenemistä) esiintyy;
- Pareesi, käsien, jalkojen halvaus;
- Muisti ja keskittymiskyky ovat heikentyneet;
- Ajatusprosessit ovat heikentyneet;
- Käytöshäiriöitä on ilmaantunut.
Alkuvaiheessa oireet ovat käytännössä poissa tai ne ovat niin merkityksettömiä, etteivät ne herätä huomiota. Tästä syystä asiantuntijat suosittelevat voimakkaasti säännöllisiä ennaltaehkäiseviä tutkimuksia ja tarkastuksia. Loppujen lopuksi mitä aikaisemmin kasvainprosessi havaitaan, sitä suuremmat ovat paranemis- ja selviytymismahdollisuudet. [ 5 ]
Aivojen gliooma lapsella
Lapsuusiässä löydetyistä monista aivokasvaimista glioomien osuus vaihtelee 15–25 prosentin välillä. Lapset voivat sairastua tautiin varhaisteini-iässä ja parikymppisenä, vaikka alle 3-vuotiailla vauvoilla tauti on hyvin harvinaista.
Patologia alkaa gliasolujen mutaation taustalla. Tähän mennessä ei ole vastausta kysymykseen, miksi tämä mutaatio tapahtuu.
Ainoa luotettavasti opittu asia on, että tietyt perinnölliset sairaudet, joihin liittyy lisääntynyt kasvainkasvun riski, lisäävät myös aivogliooman kehittymisen todennäköisyyttä.
Lisäksi tiedemiehet ovat havainneet, että gliasoluissa voi olla eroja yksittäisissä geeneissä tai kromosomeissa. Tämän häiriön vuoksi käynnistyy mutaatiomekanismi, joka ei ole perinnöllinen. On mahdollista, että tämä tapahtuu jossakin kehityksen varhaisimmista vaiheista.
On todistettu tosiasia, että akuutin leukemian tai retinoblastooman esiintyminen lapsen historiassa tai aivojen säteilytys mistä tahansa muusta syystä lisää merkittävästi gliooman muodostumisen riskiä (tietyn ajan kuluttua).
Lapsuuden oireet riippuvat pahanlaatuisuuden asteesta ja patologisen fokuksen lokalisoinnista. Oireita on spesifisiä ja epäspesifisiä:
- Epäspesifiset oireet eivät ole "sidottuja" gliooman sijaintialueeseen. Yleisiä oireita voivat olla päänsärky, huimaus, ruokahaluttomuus, oksentelu ilman yhteyttä ruokailuun, painon lasku (tuntemattomista syistä), jatkuva väsymyksen tunne, koulumenestyksen heikkeneminen, keskittymisvaikeudet ja käytöshäiriöt. Nämä oireet johtuvat kallonsisäisten rakenteiden puristumisesta, joka voidaan selittää kasvavan massan suorana paineena, ja aivo-selkäydinnesteen kiertohäiriöllä. Aivovesikipu on mahdollinen.
- Spesifinen oireyhtymä riippuu gliasolujen patologisen pesäkkeen välittömästä sijainnista. Esimerkiksi pikkuaivokasvaimeen liittyy lapsilla yleensä kävelyn ja tasapainon heikkeneminen. Suurten aivojen vaurio ilmenee kouristuskohtauksina ja selkäytimen kasvaimen kasvuna lihashalvauksena. Saattaa käydä niin, että vauvan näkö heikkenee jyrkästi, tajunta häiriintyy, uni heikkenee tai ilmenee jokin muu kehitysongelma.
Yleensä lapsuudessa pahanlaatuinen gliooma ilmenee muutaman viikon tai kuukauden kuluessa kehityksestään: sille on usein ominaista kasvaimen nopea ja hallitsematon kasvu.
Pahanlaatuisia gliakasvaimia sairastavia lapsia hoitavat lasten onkologiaan erikoistuneet lasten kliiniset keskukset. Yleensä käytetään kirurgista hoitoa, sädehoitoa ja kemoterapiaa.
Tärkein hoitovaihe on neurokirurgia. Mitä radikaalimpi se on, sitä paremmat ovat lapsen mahdollisuudet parantua. Kirurginen toimenpide ei kuitenkaan ole aina mahdollinen: ongelmia voi ilmetä erityisesti aivorungon glioomien poistossa sekä alle 3-vuotiaiden lasten sädehoidossa.
Keskusaivojen (väliaivojen ja keskiaivojen) glioomia on vaikea poistaa kokonaan, koska on olemassa terveen kudoksen vaurioitumisriski. Jos kasvaimen täydellinen poisto ei ole mahdollista, potilaalle määrätään palliatiivista hoitoa.
Pahanlaatuisia glioomia sairastavia lapsia hoidetaan standardoitujen protokollien mukaisesti, jotka on määritetty tiukasti kontrolloiduissa kliinisissä tutkimuksissa. Yleisimmät protokollat ovat seuraavat:
- HIT HGG 2007: käsittelee 3–17-vuotiaiden lasten hoitoa.
- HIT SKK: sopii vauvoille (enintään kolmevuotiaille) eikä sisällä sädehoitoja.
Gliooman lasten eloonjäämistilastot eivät yleensä ole kovin optimistisia. Hoitotoimenpiteiden tehokkuutta tietyllä lapsella ei kuitenkaan voida missään tapauksessa ennustaa etukäteen. On tärkeää noudattaa huolellisesti kaikkia lääkärin määräyksiä, mikä lisää merkittävästi toipumismahdollisuuksia.
Lomakkeet
Glioomat voivat olla lievästi pahanlaatuisia ja korkeasti pahanlaatuisia, ja niillä voi olla voimakas kasvu ja alttius etäpesäkkeille. On tärkeää ymmärtää, että lievä pahanlaatuisuus ei ole sama asia kuin kasvaimen turvallisuus. Mikä tahansa aivokasvain luo lisää tilavuutta, puristaa aivorakenteita, mikä johtaa niiden siirtymiseen ja lisääntyneeseen kallonsisäiseen paineeseen. Seurauksena potilas voi kuolla.
Pahanlaatuisia astrosytoomatyyppejä on kaksi. Nämä ovat glioblastoomat ja anaplastiset astrosytoomat, jotka jaetaan edelleen molekyylitason muutosten mukaan. Astrosytoomasta kehittyneitä sekundaarisia pahanlaatuisia kasvaimia, joilla on alhainen pahanlaatuisuusaste, esiintyy useimmiten nuorilla potilailla. Aluksi pahanlaatuisia gliasolutyyppisiä kasvaimia esiintyy useammin iäkkäillä potilailla.
Rakenteellisesta sijainnista riippuen glioomia on jaettu seuraaviin ryhmiin:
- Supratentoriaalinen (lokalisoituu pikkuaivojen yläpuolelle sivukammioiden, suurten aivopuoliskojen alueella);
- Subtentoriaalinen (lokalisoituu pikkuaivojen alapuolelle takaosan kallonpohjassa).
Histologisten ominaisuuksien mukaan erottaa tällaiset glioomityypit:
- Astrosyyttinen gliooma on yleisin. Se puolestaan jaetaan nodulaariseen ja diffuusiin glioomaan (jälkimmäiselle on ominaista nopea kasvu ja aivohalvauskuvio).
- Oligodendrogliooma - esiintyy 5 %:lla potilaista. Siinä on petrifikaatteja - kalkkeutumisalueita, useimmiten otsalohkossa.
- Ependymaalinen gliooma - kasvaa selkäytimen ja kammioiden keskuskanavan seinämiä reunustavista rakenteista. Usein kasvaa aivojen aineen paksuuteen sekä aivojen luumeniin.
Sekalaiset patologiset fokukset, kuten subependymooma, oligoastrosytooma jne., ovat myös mahdollisia.
Kaikki glioomat luokitellaan seuraaviin vaiheisiin:
- Hitaasti kasvavat suhteellisen hyvänlaatuiset kasvaimet ilman selviä kliinisiä oireita.
- Hitaasti kasvavat "rajatapaus"glioomat, jotka muuttuvat vähitellen vaiheeseen III ja sen yli.
- Pahanlaatuinen gliooma.
- Pahanlaatuinen gliooma, jolla on voimakasta ja aggressiivista kasvua ja leviämistä, huono ennuste.
Mitä alempi pahanlaatuisuusaste on, sitä pienempi on poistetun kasvaimen etäpesäkkeiden ja uusiutumisen todennäköisyys ja sitä suuremmat ovat potilaan paranemismahdollisuudet. Suurimman vaaran aiheuttaa glioblastooma multiforme, matalasti erilaistunut prosessi, jolla on voimakas kasvu ja kehitys. [ 6 ]
Mahdolliset ja yleisimmät neuroglioman variantit:
- Aivorunko- ja siltavaurioita sisältävä gliooma sijaitsee alueella, jossa aivot yhdistyvät selkäytimeen. Siellä sijaitsevat tärkeät hengitys-, sydän- ja motoriikasta vastaavat neurokeskukset. Jos tämä alue vaurioituu, tasapainoelimen ja puhelaitteen toiminta häiriintyy. Se havaitaan usein lapsuudessa.
- Näköhermoa ympäröivät neurogliasolut vaikuttavat näköhermoon. Patologia aiheuttaa näkövammaa ja eksoftalmosta. Se kehittyy useammin lapsilla.
- Matalalle pahanlaatuiselle neuroglioomalle on ominaista hidas kasvu, joka paikantuu useammin suuriin aivopuoliskoihin ja pikkuaivoihin. Se esiintyy useammin nuorilla (noin 20-vuotiailla nuorilla ja nuorilla aikuisilla).
- Aivokurkiaisen gliooma on tyypillisempi 40–60-vuotiaille henkilöille, ja sitä edustaa yleisimmin glioblastooma.
- Kiasman gliooma sijaitsee näköhermon liitoskohdassa, joten siihen liittyy likinäköisyyttä, näkökentän heikkenemistä, okklusiivista vesipäätä ja neuroendokriinisiä häiriöitä. Se voi esiintyä missä iässä tahansa, mutta yleisimmin se vaikuttaa potilaisiin, joilla on tyypin I neurofibromatoosi.
Komplikaatiot ja seuraukset
Vähäisen pahanlaatuisuuden omaavat glioomat (luokka I-II, erittäin pahanlaatuiset - esim. astrosytooma, oligoastrosytooma, oligodendrogliooma, pleomorfinen ksantoastrosytooma jne.) ja korkean pahanlaatuisuuden omaavat glioomat (luokka III-IV - glioblastooma, anaplastinen oligodendrogliooma, oligoastrosytooma ja astrosytooma). Luokan IV glioomat ovat erityisen pahanlaatuisia.
Aivorungon gliooma on ennusteeltaan erittäin epäsuotuisa juuri siksi, että kasvain vaikuttaa juuri tähän aivojen alueeseen, jossa aivojen ja raajojen väliset tärkeimmät hermoyhteydet ovat keskittyneet. Jopa melko pieni kasvain tällä alueella riittää pahentamaan potilaan tilaa nopeasti ja aiheuttamaan halvaantumisen.
Yhtä epäsuotuisia seurauksia esiintyy, kun muut aivoalueet ovat vaurioituneet. Usein kyseessä on aivokuoren kasvain, joka ei anna potilaalle pitkää elinikää hoidosta huolimatta. Usein on mahdollista vain lykätä kuolemaa.
Lääketieteellisten tilastojen mukaan viiden vuoden eloonjäämisaste on usein vain 10–20 %. Vaikka nämä luvut riippuvatkin suurelta osin sekä pahanlaatuisuuden asteesta että suoritetun kirurgisen toimenpiteen tarkasta sijainnista ja määrästä. Patologisen fokuksen täydellisen poistamisen jälkeen eloonjäämisaste kasvaa merkittävästi (joskus jopa 50 %). Hoidon puute tai sen mahdottomuus (jostain syystä) johtaa taatusti potilaan kuolemaan.
Suurin osa matalan pahanlaatuisista gliasolukasvaimista pystyy tunkeutumaan aivokudokseen ja pahanlaatumaan useiden vuosien aikana.
Asiantuntijat pitävät gliooman uusiutumisriskiä "erittäin todennäköisenä". Hoitoa ei kuitenkaan pidä laiminlyödä: on tärkeää varmistaa hyvä elämänlaatu mahdollisimman pitkään.
Uusiutuvilla glioomilla on aina huonompi ennuste kuin primaarisilla kasvaimilla. Nykyaikaiset hoitoprotokollat, jotka perustuvat terapeuttisen optimoinnin tutkimuksiin, saavuttavat kuitenkin usein riittävän hyviä tuloksia potilailla, joilla on erittäin pahanlaatuisia kasvaimia.
Mahdolliset tulokset kemoterapian jälkeen:
- Laihtuminen, niukeneminen, ruoansulatuskanavan häiriöt, suun sairaudet;
- Keskushermoston lisääntynyt herkkyys, astenia;
- Kuulon heikkeneminen, tinnitus ja korvien soiminen;
- Kouristukset, masennushäiriöt;
- Hypertensiivinen kriisi, verenkuvan muutos;
- Munuaisten vajaatoiminta;
- Allergiset prosessit, hiustenlähtö, pigmenttipaikkojen esiintyminen kehossa.
Kemoterapian jälkeen potilaat huomaavat immuunijärjestelmän voimakkaan heikkenemisen, mikä voi aiheuttaa erilaisten tartuntatautien kehittymistä.
Diagnostiikka aivojen glioomat
Aivojen glioomaa voidaan epäillä seuraavista oireista:
- Potilaalla on paikallisia tai yleistyneitä kohtauksia, jotka ovat tyypillisiä kasvaimen kortikaaliselle sijainnille ja sen hitaalle kehitykselle. Epilepsiakohtauksia esiintyy 80 %:lla potilaista, joilla on matala-asteisia gliakasvaimia, ja 30 %:lla potilaista, joilla on korkea-asteisia glioomia.
- Kohonnut kallonsisäinen paine on erityisen tyypillistä oikean otsalohkon ja päälaenlohkon kasvaimille. Korkeaan kallonsisäiseen paineeseen liittyvä verenkierron ja nesteen kierron häiriö aiheuttaa jatkuvaa ja lisääntyvää päänsärkyä, pahoinvointia ja oksentelua, näköhäiriöitä ja uneliaisuutta. Esiintyy näköhermon turvotusta ja suuntaavan hermon halvaantumista. Kallonsisäisen paineen nousu kriittisille arvoille voi johtaa koomaan ja kuolemaan. Toinen korkean silmänpaineen syy on vesipää.
- Potilaalla on kasvava fokaalinen kuva. Supratentoriaalisissa muodostelmissa motoriset ja aistilliset sfäärit ovat häiriintyneet, hemiopia, afasia ja kognitiiviset häiriöt etenevät.
Jos lääkäri epäilee aivokasvaimen läsnäoloa, on optimaalista suorittaa magneettikuvaus ilman varjoainetta (gadoliniumia) tai sen kanssa, jotta voidaan selvittää sen sijainti, koko ja lisäominaisuudet. Jos magneettikuvaus ei ole mahdollista, suoritetaan tietokonetomografia ja magneettiresonanssispektroskopiaa käytetään erilaistumismenetelmänä. Näiden diagnostisten menetelmien informatiivisuudesta huolimatta lopullinen diagnoosi tehdään vasta histologisen vahvistuksen jälkeen kasvainfektion resektiossa.
Yllä olevien kriteerien perusteella on suositeltavaa aloittaa diagnoosi perusteellisella anamneesilla, somatoneurologisen tilan ja toimintakyvyn arvioinnilla. Neurologisen tilan arvioinnissa määritetään mahdolliset älylliset ja henkiset häiriöt.
Suositellut laboratoriotestit:
- Täysimittainen yleinen kliininen verikoe;
- Täydellinen verikemian paneeli;
- Virtsa-analyysi;
- Veren hyytymistutkimus;
- Onkologisten merkkiaineiden analyysi (AFP, beeta-hCG, LDH - merkityksellisiä, jos epäillään käpylisäkkeen leesiota).
Glioblastoomaa ja anaplastista astrosytoomaa sairastavien potilaiden ennustearvojen selventämiseksi arvioidaan IDH1|2-1-geenin mutaatiota ja MGMT-geenin metylaatiota. Oligodendroglioomaa ja oligoastrosytoomaa sairastavilla potilailla määritetään 1p|19q-koodelaatio.
Instrumentaalinen diagnostiikka on ensisijaisesti aivojen (joskus ja selkäytimen) pakollinen magneettikuvaus. Magneettikuvaus suoritetaan kolmessa projektiossa käyttäen standardeja T1-2-, FLAIR- ja T1-tiloja varjoaineen kanssa.
Tarvittaessa suoritetaan verisuoniverkoston ultraäänitutkimus, motoristen ja puheosien toiminnallinen magneettikuvaus sekä angiografia, spektroskopia, MR-traktografia ja perfuusio.
Lisätutkimuksiin voi sisältyä:
- Aivojen elektroenkefalografia;
- Konsultaatiot neurokirurgin, onkologin, radiologin, silmälääkärin ja radiologin kanssa.
Differentiaalinen diagnoosi
Differentiaalidiagnoosi suoritetaan välttämättä ei-kasvainpatologioissa - erityisesti arteriovenoosisen tai valtimoiden epämuodostuman aiheuttamassa verenvuodossa sekä pseudotumoraalisissa demyelinaatioprosesseissa, tulehdussairauksissa (toksoplasmoosi, aivopaise jne.).
Lisäksi erottaa ensisijainen kasvaimen keskittyminen ja keskushermoston etäpesäkkeet.
Nykyaikaisilla magneettikuvausmenetelmillä on mahdollista suorittaa diagnostisia toimenpiteitä riittävän tarkasti, jotta voidaan selvittää primaaripesäkkeen alkuperä keskushermostossa. Aivojen magneettikuvaus tehdään varjoaineella tai ilman, T1- ja T2-FLAIR-tilassa – kolmessa projektiossa – tai ohuina viipaleina aksiaalisessa projektiossa (SPGR-tilassa). Nämä diagnostiset menetelmät mahdollistavat kasvaimen sijainnin, koon, rakenteellisten ominaisuuksien, sen suhteen verisuoniverkostoon ja lähellä oleviin aivoalueisiin määrittämisen tarkasti.
Lisäksi osana erotusdiagnoosia voidaan suorittaa TT-kuvaus (varjoaineella tai ilman), TT-angiografia (MR-angiografia), MR-traktografia sekä MR- tai TT-perfuusio. Aivojen TT/PET-kuvausta metioniinilla, koliinilla, tyrosiinilla ja muilla aminohapoilla käytetään tarvittaessa.
Hoito aivojen glioomat
Spesifinen hoito koostuu kirurgisista, kemoterapia- ja sädehoitotoimenpiteistä. Kasvaimen täydellinen poisto on pakollista, jos mahdollista, mikä mahdollistaa oireiden nopean lievityksen ja diagnoosin histologisen vahvistamisen.
Säteilytyksellä on positiivinen vaikutus potilaiden elinajanodotteen pidentämiseen. Tavallisesti annetaan 58–60 Gy:n kokonaisannos, joka jaetaan yksittäisiin 1,8–2 Gy:n säteilyannoksiin. Kasvainta säteilytetään paikallisesti ja lisäksi valoa siepataan jopa 3 cm sen ympäriltä. Sädehoito on hyväksyttävämpi vaihtoehto kuin brachyterapia. Joissakin tapauksissa suositellaan radiosurgisia menetelmiä, joihin kuuluvat säteilytys gammaveitsellä tai lineaarisella kaasupolkimella, sekä neutronikaappausboorihoito.
Adjuvanttikemoterapian tarve on kiistanalainen. Joissakin tapauksissa nitrosoureavalmisteet ovat pidentäneet potilaiden elinajanodottetta jopa puoleentoista vuoteen, mutta jotkut tällaisten kemoterapiavalmisteiden käytön tulokset ovat olleet negatiivisia. Nykyään käytetään aktiivisesti sytotoksisia aineita, neoadjuvanttihoitoa (ennen sädehoitoa), yhdistelmälääkkeitä, valtimoiden sisäistä kemoterapiaa tai suuriannoksista kemoterapiaa, johon liittyy edelleen kantasolusiirtoja.
Yleisesti ottaen glioomien onnistuneen hoidon kannalta kokonaisvaltainen lähestymistapa on erittäin tärkeä, ja sen laajuus riippuu kasvaimen sijainnista ja pahanlaatuisuuden asteesta, koosta sekä potilaan yleisestä terveydentilasta.
Aivorungon gliooman yhteydessä kirurgista toimenpidettä käytetään harvoin. Leikkauksen pääasiallinen vasta-aihe on pesäkkeen sijainti – lähellä elintärkeitä osia. Joissakin tapauksissa vartalon gliooma on mahdollista poistaa mikrokirurgisilla menetelmillä, preoperatiivisella ja postoperatiivisella kemoterapialla. Tällainen toimenpide on hyvin monimutkainen ja vaatii neurokirurgin erityispätevyyttä.
Sädehoito ja erityisesti stereotaktinen leikkaus, jossa altistutaan suurille ionisoiville annoksille, on varsin tehokasta. Tällaisen tekniikan käyttö kasvaimen kehityksen alkuvaiheessa mahdollistaa joskus pitkäaikaisen remission tai jopa potilaan täydellisen paranemisen.
Sädehoito yhdistetään usein kemoterapiaan, mikä parantaa toimenpiteiden tehoa ja vähentää säteilykuormitusta. Glioomassa kaikki kemopreventiiviset aineet eivät ole terapeuttisesti tehokkaita, joten ne määrätään yksilöllisesti ja lääkemääräyksiä muutetaan tarvittaessa.
Kivun vähentämiseksi ja kallonsisäisen paineen alentamiseksi, riippumatta pääasiallisesta hoidosta, määrätään oireenmukaista hoitoa - erityisesti kortikosteroidilääkkeitä, kipulääkkeitä, rauhoittavia lääkkeitä.
Lääkkeet
Kortikosteroidilääkkeet vaikuttavat turvotukseen ja lievittävät neurologisten oireiden vakavuutta useiden päivien ajan. Useiden sivuvaikutusten ja solunsalpaajalääkkeiden kanssa esiintyvien haitallisten yhteisvaikutusten todennäköisyyden lisääntymisen vuoksi käytetään kuitenkin mahdollisimman tehokkaita steroidiannoksia, jotka lopetetaan mahdollisimman pian (esim. leikkauksen jälkeen).
Kouristuslääkkeitä käytetään systemaattisesti toissijaisena ehkäisytoimenpiteenä potilailla, joilla on jo ollut epileptisiä kohtauksia. Nämä lääkkeet voivat aiheuttaa vakavia haittavaikutuksia ja myös olla yhteisvaikutuksessa solunsalpaajien kanssa.
Antikoagulantit ovat erityisen tärkeitä leikkauksen jälkeisessä vaiheessa, koska tromboflebiitin muodostumisen riski glioomassa on melko korkea (jopa 25%).
Masennuslääkkeiden ja anksiolyyttien ottamisesta odotetaan hyvää vaikutusta. Metyylifenidaatin käyttö 10–30 mg/vrk kahtena annoksena mahdollistaa usein kognitiivisten kykyjen optimoinnin, elämänlaadun parantamisen ja työkyvyn ylläpitämisen.
Neurologinen vajaatoiminta ja aivoödeeman merkit (päänsärky, tajunnan häiriöt) eliminoituvat kortikosteroidilääkkeillä - erityisesti prednisolonilla tai deksametasonilla. |
Kortikosteroidien hoito-ohjelma ja annostus valitaan yksilöllisesti käyttäen pienintä tehokasta annosta. Hoitojakson lopussa lääkkeet poistetaan vähitellen. |
Kortikosteroideja otetaan yhdessä mahalaukkua suojaavien lääkkeiden - protonipumpun salpaajien tai H2-histamiinireseptorin salpaajien - kanssa. |
Diureetteja (furosemidi, mannitoli) määrätään aivorakenteiden vakavaan turvotukseen ja siirtymään kortikosteroidilääkkeiden lisänä. |
Jos potilaalla ilmenee kouristuskohtauksia (mukaan lukien anamneesi) tai aivosähkökäyrässä havaittavia epileptiformisia oireita, määrätään lisäksi kouristuslääkitystä. Kouristuslääkkeitä ei määrätä ennaltaehkäiseviin tarkoituksiin. |
Potilaille, joilla on kemoterapiaa koskevia indikaatioita, suositellaan antikonvulsiivisia lääkkeitä, jotka eivät vaikuta maksaentsyymien toimintaan. Suositellut lääkkeet: Lamotrigiini, Valproiinihappo, Levetirasetaami. Ei tule käyttää: Karbamatsepiinia, Fenobarbitaalia. |
Aivoglioomien aiheuttamaa päänsärkyä hoidetaan kortikosteroideilla. |
Joissakin päänsärkytapauksissa voidaan käyttää tulehduskipulääkkeitä tai tramadolia. |
Jos potilas käyttää tulehduskipulääkkeitä (NSAID), ne lopetetaan muutamaa päivää ennen leikkausta leikkauksen aikaisen verenvuodon riskin minimoimiseksi. |
Valituissa kiputapauksissa voidaan suositella narkoottisia kipulääkkeitä, kuten fentanyyliä tai trimeperidiiniä. |
Keuhkoembolian estämiseksi kolmannesta leikkauksen jälkeisestä päivästä lähtien on määrätty pienimolekyylipainoisten hepariinien - erityisesti natriumenoksapariininatriumin tai kalsiumin - anto. |
Jos potilas käyttää systemaattista antikoagulantti- tai antiaggreganttihoitoa, hänet siirretään pienimolekyylipainoisiin hepariineihin viimeistään viikkoa ennen leikkausta, ja niiden lopettaminen leikkausta edeltävänä päivänä ja jatkaminen 24–48 tuntia leikkauksen jälkeen. |
Jos glioomapotilaalla on alaraajojen laskimotukos, hoito suoritetaan suorilla antikoagulanteilla. CAVA-suodattimen asentamisen mahdollisuutta ei suljeta pois. |
Kemoterapia aivojen pahanlaatuisiin glioomiin
Gliooman peruskasvainten vastaiset kemoterapiaohjelmat katsotaan olevan:
- Lomustiini 100 mg/m² ensimmäisenä päivänä, vinkristiini 1,5 mg/m² ensimmäisenä ja kahdeksantena päivinä, prokarbatsiini 70 mg/m² kahdeksannesta päivästä kahdenteenkymmenenteenensimmäiseen, hoitojaksot kuuden viikon välein.
- Lomustiini 110 mg/m² kuuden viikon välein.
- Temotsolomidi 5/23 150–200 mg/m² päivästä yksi viiteen, 28 päivän välein.
- Temotsolomidia osana kemo- ja sädehoitoa, 75 mg/m² joka päivä, jona sädehoitoa annetaan.
- Temotsolomidia yhdessä sisplatiinin tai karboplatiinin (80 mg/m²) kanssa ja temotsolomidia 150–200 mg/m² päivinä 1–5 neljän viikon välein.
- Temotsolomidi 7/7 annoksella 100 mg/m² kuurin päivinä 1–8 ja 15–22, ja toistetaan neljän viikon välein.
- Bevasitsumabia 5–10 mg/kg päivinä yksi ja viisitoista ja irinotekaania 200 mg/m² päivinä yksi ja viisitoista, toistettuna neljän viikon välein.
- Bevasitsumabia 5–10 mg/kg päivinä yksi, viisitoista ja kaksikymmentäyhdeksän ja lomustiinia 90 mg/m² päivänä yksi kuuden viikon välein.
- Bevasitsumabi 5–10 mg/kg päivinä yksi ja viisitoista, lomustiini 40 mg päivinä yksi, kahdeksan, viisitoista ja kaksikymmentäkaksi, toistettuna kuuden viikon välein.
- Bevasitsumabi 5–10 mg/kg päivinä yksi ja viisitoista, toistettuna neljän viikon välein.
Sytostaattiset lääkkeet estävät monissa tapauksissa onnistuneesti kasvainsolujen kasvua, mutta eivät osoita selektiivisyyttä terveitä kudoksia ja elimiä kohtaan. Siksi asiantuntijat ovat tunnistaneet useita vasta-aiheita, joissa gliooman kemoterapia on mahdotonta:
- Liiallinen yksilöllinen herkkyys kemopreventiivisille aineille;
- Sydämen, munuaisten ja maksan toiminnan dekompensointi;
- Masentunut hematopoieesi luuytimessä;
- Lisämunuaisten toimintahäiriöt.
Kemoterapiaa annetaan äärimmäisen varoen:
- Potilaat, joilla on merkittäviä sydämen rytmihäiriöitä;
- Diabeteksen kanssa;
- Akuuteissa virusinfektioissa;
- Iäkkäille potilaille;
- Kroonisesta alkoholismista (kroonisesta alkoholimyrkytyksestä) kärsivät potilaat.
Kemopreventiivisten lääkkeiden vakavin sivuvaikutus on niiden myrkyllisyys: sytostaatit häiritsevät selektiivisesti verisolujen toimintaa ja muuttavat niiden koostumusta. Seurauksena verihiutaleiden ja punasolujen massa vähenee ja kehittyy anemia.
Ennen kemoterapian määräämistä lääkäri ottaa aina huomioon lääkkeiden myrkyllisyyden asteen ja todennäköiset komplikaatiot niiden käytön jälkeen. Kemoterapiakuureja seurataan aina tarkasti asiantuntijoiden toimesta ja verikokeilla tehdään säännöllisiä seurantatoimia.
Sytostaattihoidon mahdolliset seuraukset:
- Laihtuminen, laihtuminen;
- Nielemisvaikeudet, kuivat limakalvot, parodontiitti, dyspepsia;
- Keskushermoston epävakaus, maaniset ja masennushäiriöt, kouristusoireyhtymä, astenia;
- Kuulotoiminnan heikkeneminen;
- Verenpaineen nousu hypertensiivisen kriisin kehittymiseen asti;
- Verihiutaleiden, punasolujen, valkosolujen väheneminen, useita verenvuotoja, sisäinen ja ulkoinen verenvuoto;
- Munuaisten vajaatoiminta;
- Allergiset prosessit;
- Hiustenlähtö, lisääntyneen pigmentaation alueiden ulkonäkö.
Kemoterapiajaksojen jälkeen potilailla on lisääntynyt riski sairastua tartuntatauteihin, ja lihas- ja nivelkivut ovat yleisiä.
Kemoterapian jälkeisten haitallisten vaikutusten riskin vähentämiseksi on välttämättä määrättävä lisäkuntoutustoimenpiteitä, joiden tarkoituksena on palauttaa normaali verenkuva, vakauttaa sydän- ja verisuonitoiminta ja normalisoida neurologinen tila. Riittävä psykologinen tuki on välttämätöntä.
Kirurginen hoito
Leikkaus suoritetaan kasvaimen keskittymisen poistamiseksi mahdollisimman paljon, mikä puolestaan pitäisi vähentää kallonsisäistä painetta, vähentää neurologista vajaatoimintaa ja tarjota tarvittava biomateriaali tutkimukselle.
- Leikkaus suoritetaan erikoistuneessa neurokirurgisessa osastolla tai klinikalla, jonka asiantuntijoilla on kokemusta neuroonkologisista toimenpiteistä.
- Kirurgi suorittaa pääsyn plastisella luutrepanaatiolla epäillyn gliooman lokalisaation alueelle.
- Jos kasvain sijaitsee anatomisesti lähellä motorisia alueita tai ratoja, tai tumakkeissa tai aivohermojen varrella, käytetään leikkauksen jälkeistä neurofysiologista seurantaa.
- Neuronavigoinnissa intraoperatiivinen fluoresenssinavigointi 5-aminolevuleenihapolla on toivottavaa kasvaimen poiston maksimoimiseksi.
- Toimenpiteen jälkeen tehdään kontrollina TT- tai MRI-kuvaus (varjoaineen injektiolla tai ilman) päivinä 1–2.
Jos gliooman kirurginen resektio on mahdotonta tai aluksi todetaan epätarkoituksenmukaiseksi tai jos epäillään keskushermoston lymfoomaa, suoritetaan biopsia (avoin, stereotaktinen, navigointiseuranta jne.). |
Aivogliomatoosia sairastavat potilaat varmennetaan stereotaktisella biopsialla, koska hoitotaktiikat riippuvat suurelta osin histologisesta kuvasta. |
Tietyissä tilanteissa – iäkkäillä potilailla, vakavien neurologisten häiriöiden yhteydessä, gliooman lokalisoituessa vartalossa ja muissa elintärkeissä osissa – hoito suunnitellaan oireiden ja kuvantamistietojen perusteella yleisen lääkärin konsultaation jälkeen. |
Potilaille, joilla on piloidinen astrosytooma sekä aivorungon nodulaariset kasvaimet ja eksofyyttiset prosessit, suositellaan resektiota tai avointa biopsiaa. |
Potilaita, joilla on diffuusi pontiinigliooma ja muita vartalon diffuuseja kasvaimia, hoidetaan sädehoidolla ja lääkehoidolla. Tällaisissa tapauksissa varmennusta ei tarvita. |
Potilaille, joilla on neliraajahalvaantunut levyglioma, tehdään systemaattinen magneettikuvaus ja kliininen seuranta aivovesikivespotilaksen poiston jälkeen. Jos kasvain osoittaa kasvun merkkejä, se poistetaan ja sädetetään uudelleen. |
Kun suoritetaan matala-asteisen pahanlaatuisen gliooman osittainen resektio tai biopsia, potilaita, joilla on kaksi tai useampia riskitekijöitä, hoidetaan välttämättä sädehoidolla ja/tai kemoterapialla. |
Täydellinen resektio on pakollinen potilaille, joilla on subependymaalinen jättisoluinen astrosytooma. |
Everolimuusia määrätään diffuusin subependymaaliseen jättisoluastrosytoomaan. |
Piloidiastrosytooma tulee poistaa magneettikuvauksella intervention jälkeen kasvainkudoksen radikaalin resektion laadun selvittämiseksi. |
Glioblastoomassa leikkauksen jälkeinen hoito (sädehoito + kemoterapia) tulee yhdistää temotsolomidin antoon. |
Leikkauksen jälkeisessä anaplastisessa astrosytoomassa on aiheellista sädehoitoa ja jatkohoitoa lääkehoidolla. Käytetään lomustiinia ja temotsolomidia. |
Anaplastista oligodendroglioomaa tai oligoastrosytoomaa sairastavat potilaat saavat leikkauksen jälkeen sekä sädehoitoa että kemoterapiaa (Temozolomidia tai PCV-monoterapiaa). |
Iäkkäille potilaille, joilla on laaja-alainen, pahanlaatuinen gliooma, annetaan sädehoitoa hypofraktionoidulla tavalla tai temotsolomidimonoterapiaa. |
Gliooman uusiutuessa asiantuntijaryhmä keskustelee uusintaleikkauksen mahdollisuudesta ja sitä seuraavista hoitotaktiikoista. Optimaalinen hoito uusiutuessa: uusintaleikkaus + systeeminen kemoterapia + toistuva sädehoito + palliatiiviset toimenpiteet. Jos kasvaimen uusiutumista esiintyy paikallisesti pienissä kohdissa, voidaan käyttää sädehoitoa. |
Uusiutuvan glioomakasvun hoitoon ensisijaisesti käytettäviä lääkkeitä ovat temotsolomidi ja bevasitsumabi. |
Erittäin pahanlaatuisten oligodendroglioomien ja anaplastisten astrosytoomien uusiutuminen on temotsolomidihoidon aihe. |
Pleomorfinen ksantoastrosytooma poistetaan ilman pakollista adjuvanttia kemoterapiaa. |
Yksi glioomien erityispiirteistä on niiden hoidon ja poiston vaikeus. Kirurgi pyrkii poistamaan kasvaimen kudokset mahdollisimman täydellisesti tilan kompensoimiseksi. Monet potilaat pystyvät parantamaan elämänlaatua ja pidentämään sitä, mutta erittäin pahanlaatuisten kasvainten ennuste on edelleen epäsuotuisa: patologisen pesäkkeen uudelleenkasvun todennäköisyys on lisääntynyt.
Ravitsemus aivojen glioomalle
Ruokavalio pahanlaatuisia kasvaimia sairastaville potilaille - tärkeä asia, johon valitettavasti monet ihmiset eivät kiinnitä paljon huomiota. Samaan aikaan ruokavalion muutosten ansiosta on mahdollista hidastaa gliooman kehittymistä ja vahvistaa ja horjuttaa immuniteettia.
Ruokavalion muutoksen pääkohdat:
- Aineenvaihduntaprosessien normalisointi, immuunipuolustuksen vahvistaminen;
- Kehon vieroitus;
- Energiapotentiaalin optimointi;
- Varmistaa kaikkien elinten ja kehon järjestelmien normaalin toiminnan heille niin vaikeana aikana.
Rationaalinen ja tasapainoinen ruokavalio on välttämätön sekä potilailla, joilla on pahanlaatuisia kasvaimia varhaisessa vaiheessa että potilailla, joilla on glioblastooman viimeinen vaihe. Huolellisesti valittu ruokavalio edistää yleisen hyvinvoinnin paranemista ja vaurioituneiden kudosten toipumista, mikä on erityisen tärkeää sytostaatti- ja sädehoidon taustalla. Ravintoaineiden tasapaino ja oikeanlaiset aineenvaihduntaprosessit estävät infektiopesäkkeiden muodostumisen, estävät tulehdusreaktioita ja ehkäisevät elimistön uupumusta.
Seuraavia ruokia ja juomia suositellaan aivoglioomaan:
- Punaiset, keltaiset ja oranssinväriset hedelmät ja vihannekset (tomaatit, persikat, aprikoosit, porkkanat, punajuuret, sitrushedelmät), jotka sisältävät karotenoideja, jotka suojaavat terveitä soluja sädehoidon kielteisiltä vaikutuksilta;
- Kaali (kukkakaali, parsakaali, ruusukaali), retiisi, sinappi ja muut kasvituotteet, jotka sisältävät indolia - vaikuttavaa ainetta, joka neutraloi haitallisia myrkyllisiä ja kemiallisia tekijöitä;
- Vihreät (tilli, persilja, nuoret voikukan ja nokkosen lehdet, raparperi, rucola, pinaatti), vihreät herneet ja parsa, parsapavut ja levät (merilevä, spirulina, chlorella);
- Vihreä tee;
- Valkosipuli, sipuli, ananas, joilla on kasvaimia estävä ja vieroituskyky;
- Leseet, viljat, täysjyväleipä, itäneet palkokasvien idut, jyvät ja siemenet;
- Tummat viinirypäleet, vadelmat, mansikat ja mansikat, mustikat, karhunvatukat, granaattiomena, herukat, mustaherukat, pihlajanmarjat, mustikat, tyrnimarja, kirsikat ja muut marjat, jotka sisältävät luonnollisia antioksidantteja, jotka vähentävät vapaiden radikaalien, virusten ja karsinogeenien kielteisiä vaikutuksia;
- Vähärasvaiset maitotuotteet.
Ruoansulatusjärjestelmää ja koko kehoa ei kannata kuormittaa raskailla ja rasvaisilla ruoilla. On hyödyllistä käyttää vastapuristettuja kotitekoisia mehuja, smoothieita ja herkkupaloja. Ruokavalioihin kannattaa lisätä omega-3-rasvahappojen lähteitä, kuten kalaöljyä, pellavansiemenöljyä tai pellavansiemeniä.
Sokeria ja makeisia on parempi välttää kokonaan. Mutta lusikallinen hunajaa kupillisen veden kanssa ei tee pahaa: mehiläistuotteilla on voimakas tulehdusta estävä, antioksidanttinen ja kasvaimia estävä vaikutus. Ainoa vasta-aihe hunajan käytölle on allergia tuotteelle.
Ruokavaliosta tulisi sulkea pois:
- Liha, sianliha, sisäelimet;
- Voi, rasvaiset maitotuotteet;
- Savustettu liha, makkarat, säilykeliha ja kala;
- Alkoholi missä tahansa muodossa;
- Makeiset, leivonnaiset, kakut ja leivonnaiset, karkit ja suklaat;
- Valmisruoat, pikaruoka, välipalat;
- Paistetut ruoat.
Sinun tulisi syödä päivittäin riittävästi vihanneksia, vihanneksia, hedelmiä ja marjoja sekä juoda puhdasta vettä.
Kemoterapian aikana ja jonkin aikaa sen jälkeen sinun tulisi juoda kotitekoisia vihannes- ja hedelmämehuja, syödä kotitekoista vähärasvaista raejuustoa, maitoa ja juustoa. On tärkeää juoda runsaasti nesteitä, harjata hampaasi ja huuhdella suusi usein (noin 4 kertaa päivässä).
Optimaaliset ateriat aivoglioomapotilaille:
- Kasvispata;
- Viljasta (mieluiten tattarista, kaurapuurosta, riisistä, kuskusista, bulgurista) valmistetut lisukkeet ja keitot;
- Höyrytetyt juustokakut, vanukkaat, padat;
- Haudutetut ja paistetut vihannekset;
- Padat, kasviskeitot, palkokasveista (mukaan lukien soija) valmistetut alku- ja pääruoat, pateet ja sufleet;
- Smoothieita, vihreää teetä, kompotteja ja herkkupaloja.
Ennaltaehkäisy
Jos henkilö elää terveellistä elämäntapaa, eikä hänen sukulaistensa keskuudessa ole ollut syöpätapauksia, hänellä on kaikki mahdollisuudet olla sairastumatta aivoglioomaan. Tällaisille kasvaimille ei ole erityistä ehkäisyä, joten tärkeimpinä ennaltaehkäisevinä toimenpiteinä pidetään asianmukaista ravitsemusta, liikuntaa, huonojen tapojen välttämistä sekä ammatillisten ja kotitalouksien vaarojen puuttumista.
Asiantuntijat antavat useita yksinkertaisia mutta tehokkaita suosituksia:
- Juo enemmän puhdasta vettä, vältä makeutettuja virvoitusjuomia, mehuja, energiajuomia ja alkoholia.
- Vältä työperäisiä ja kotitalouksien vaaroja: vähemmän kosketusta kemikaalien, syövyttävien liuosten ja nesteiden kanssa.
- Pyri valmistamaan ruokaa keittämällä, hauduttamalla, uunissa paistamalla, mutta älä friteeraamalla. Suosi terveellisiä ja laadukkaita kotitekoisia ruokia.
- Suuri osa ruokavaliostasi tulisi olla kasvisruokaa, mukaan lukien vihreät, vuodenajasta riippumatta.
- Toinen negatiivinen tekijä on ylipaino, josta tulisi päästä eroon. Painonhallinta on erittäin tärkeää koko kehon terveydelle.
- Kasviöljyjä tulisi aina suosia voin ja sianlihan sijaan.
- Jos mahdollista, on suositeltavaa suosia ympäristöystävällisiä tuotteita, hormonitonta lihaa sekä nitraatittomia ja torjunta-aineita sisältämättömiä vihanneksia ja hedelmiä. Punaista lihaa on parempi välttää kokonaan.
- Älä ota monivitamiinivalmisteita ilman käyttöaiheita ja suuria määriä. Älä ota mitään lääkkeitä ilman lääkärin määräystä: itsehoito on usein erittäin, erittäin vaarallista.
- Jos epäilyttäviä oireita ilmenee, on tarpeen käydä lääkärissä odottamatta tilanteen pahenemista, haittavaikutusten ja komplikaatioiden kehittymistä.
- Makeiset ja korkean glykeemisen indeksin omaavat ruoat ovat ei-toivottu osa ruokavaliota.
- Mitä aikaisemmin henkilö menee lääkäreille, sitä paremmat ovat hänen mahdollisuutensa parantua (ja tämä pätee lähes kaikkiin sairauksiin, mukaan lukien aivojen gliooma).
Onkopatologian muodostumisen estämiseksi tarvitset riittävästi aikaa nukkua ja levätä, välttää alkoholijuomien liiallista kulutusta, suosia korkealaatuista luonnollista ruokaa ja vähentää gadgetien (erityisesti matkapuhelimien) käyttöä.
Kasvainsairauksia esiintyy usein iäkkäillä ja vanhoilla ihmisillä. Siksi on tärkeää seurata omaa terveyttään nuoresta iästä lähtien eikä provosoida patologisia prosesseja epäterveellisillä elämäntavoilla ja epäterveellisillä tavoilla.
Onkologian tarkkoja perimmäisiä syitä ei ole vielä selvitetty. Tietty rooli on kuitenkin myös epäsuotuisilla työ- ja ympäristöolosuhteilla, altistumisella ionisoivalle ja sähkömagneettiselle säteilylle sekä hormonaalisilla muutoksilla. Älä oleskele pitkään ja säännöllisesti auringossa, anna ympäristön lämpötilan muuttua äkillisesti, ylikuumene kylvyssä tai saunassa, ota usein kuumia kylpyjä tai suihkuja.
Toinen kysymys: miten estää aivogliooman uusiutuminen onnistuneen hoidon jälkeen? Kasvaimen kasvun uusiutuminen on monimutkainen ja valitettavasti yleinen komplikaatio, jota on vaikea ennustaa etukäteen. Potilaille voidaan suositella säännöllisiä ennaltaehkäiseviä tutkimuksia ja tarkastuksia, käyntiä onkologin ja hoitavan lääkärin vastaanotolla vähintään kaksi kertaa vuodessa, terveellisiä elämäntapoja, terveellisen ja luonnollisen ruoan syömistä sekä kohtuullista liikuntaa. Toinen edellytys on elämänrakkaus, terveellinen optimismi ja myönteinen asenne menestykseen kaikissa olosuhteissa. Tähän sisältyy myös ystävällinen ilmapiiri perheessä ja työpaikalla, kärsivällisyys ja läheisten ehdoton tuki.
Ennuste
Aivojen tila ja gliooman ominaisuudet sen havaitsemishetkellä vaikuttavat eloonjäämisasteeseen yhtä paljon kuin annettu hoito. Potilaan tyydyttävä yleisterveys ja ikä parantavat ennustetta (nuorilla potilailla ennuste on optimistisempi). Tärkeä indikaattori on kasvaimen histologinen kuva. Siten matala-asteisilla glioomilla on parempi ennuste kuin anaplastisilla glioomilla ja vielä enemmän glioblastoomilla (epäsuotuisimmat kasvainprosessit). Astrosytoomilla on huonompi ennuste kuin oligodendroglioomoilla.
Pahanlaatuiset astrosytoomat reagoivat huonosti hoitoon ja niiden eloonjäämisaste on suhteellisen alhainen, kuudesta viiteen vuotta. Samalla matala-asteisten glioomien elinajanodote on arviolta 1–10 vuotta.
Pahanlaatuiset astrosytoomat ovat pohjimmiltaan parantumattomia. Hoidon suunta on yleensä neurologisten oireiden (mukaan lukien kognitiivisten toimintahäiriöiden) vähentäminen ja elinajanodotteen pidentäminen samalla, kun elämänlaatu on mahdollisimman korkea. Oireenmukaista hoitoa tarjotaan kuntoutustoimenpiteiden taustalla. Myös psykologin työ on tärkeää.
Viimeisen vuosikymmenen aikana tiedemiehet ovat edistyneet jonkin verran aivokasvainten luonteen ja niiden hoidon ymmärtämisessä. Taudin ennusteen optimoimiseksi on tehtävä paljon enemmän. Asiantuntijoiden ensisijainen tehtävä nykyään on seuraava: aivoglioomassa tulisi olla useita järjestelmiä ongelman tehokkaaksi poistamiseksi kerralla, sekä kehityksen alkuvaiheessa että myöhemmissä vaiheissa.

