
Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Uudet geneettiset mekanismit voisivat olla terapeuttinen kohde glioomaa vastaan
Viimeksi tarkistettu: 02.07.2025
Shi-Yuan Chengin, tohtori ja Ken ja Ruth Daveyn neuroonkologian osaston professorin, laboratoriossa tekemä tutkimus on tunnistanut uusia mekanismeja, jotka ovat taustalla vaihtoehtoisille RNA:n silmukointitapahtumille glioomakasvainsoluissa ja jotka voivat toimia uusina terapeuttisina kohteina. Tutkimustulokset on julkaistu Journal of Clinical Investigation -lehdessä.
"Olemme löytäneet erilaisen tavan hoitaa glioomaa vaihtoehtoisen silmukoinnin kautta ja löytäneet uusia kohteita, joita ei ole aiemmin tunnistettu, mutta jotka ovat tärkeitä gliooman pahanlaatuisuuden kannalta", sanoo Xiao Song, lääketieteen tohtori, neurologian apulaisprofessori ja tutkimuksen pääkirjoittaja.
Glioomat ovat yleisin primaarinen aivokasvaintyyppi aikuisilla, ja ne saavat alkunsa gliasoluista, jotka sijaitsevat keskushermostossa ja tukevat viereisiä hermosoluja. Glioomat ovat erittäin resistenttejä tavanomaisille hoidoille, kuten sädehoidolle ja kemoterapialle, kasvaimen geneettisen ja epigeneettisen heterogeenisyyden vuoksi, mikä korostaa uusien terapeuttisten kohteiden löytämisen tarvetta.
Chengin laboratorion aiempi, Cancer Research -lehdessä julkaistu tutkimus osoitti, että tärkeän silmukointitekijän SRSF3:n määrä on merkittävästi koholla glioomissa verrattuna normaaleihin aivoihin, ja SRSF3:n säätelemä RNA:n silmukointi edistää glioomien kasvua ja etenemistä vaikuttamalla useisiin soluprosesseihin kasvainsoluissa.
RNA:n silmukointi on prosessi, johon liittyy intronien (RNA:n ei-koodaavien alueiden) poistaminen ja eksonien (koodaavien alueiden) yhdistäminen kypsän mRNA-molekyylin muodostamiseksi, joka tukee geenien ilmentymistä solussa.
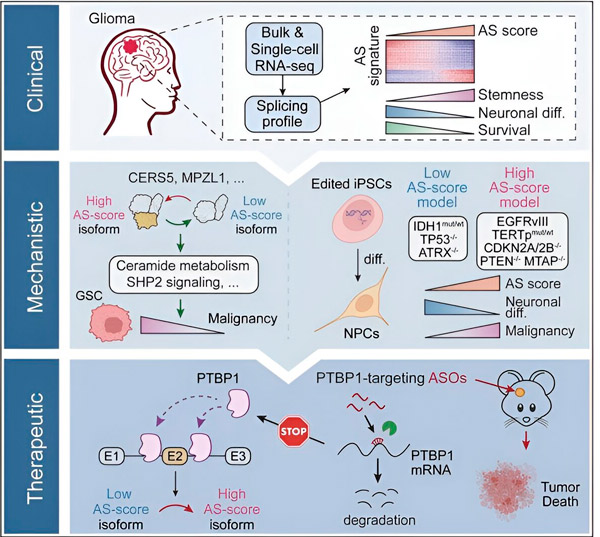
Tässä tutkimuksessa tutkijat pyrkivät tunnistamaan glioomasolujen vaihtoehtoisen silmukoinnin muutoksia, näiden muutosten taustalla olevia mekanismeja ja määrittämään niiden potentiaalin terapeuttisina kohteina.
Laskennallisten menetelmien ja RNA-sekvensointitekniikoiden avulla tutkijat tarkastelivat potilasnäytteistä saatujen glioomakasvainsolujen silmukointimuutoksia. Näiden muutosten vahvistamiseksi he käyttivät CRISPR-geeninmuokkaustekniikoita tuodakseen erilaisia glioomaa ohjaavia mutaatioita ihmisen indusoiduista pluripotenteista kantasoluista (iPSC) johdettuihin glioomamalleihin.
He havaitsivat, että näitä silmukointimuutoksia tehostaa epidermaalisen kasvutekijäreseptorin III (EGFRIII) variantti, jonka tiedetään ilmentyvän yli monissa kasvaimissa, mukaan lukien glioomissa, ja että niitä estää IDH1-geenin mutaatio.
Tutkijat ovat vahvistaneet kahden RNA:n silmukointitapahtuman toiminnan, jotka luovat erilaisia proteiini-isoformeja, joilla on erilaiset aminohapposekvenssit.
"Vain yksi näistä isoformeista voi edistää kasvaimen kasvua, toisin kuin toinen isoformi, jota normaalisti ilmentyy normaalissa aivoissa. Kasvaimet hyödyntävät tätä mekanismia ilmentääkseen selektiivisesti kasvainta edistävää isoformia normaalin aivoisoformin sijaan", Song sanoi.
Tutkimusryhmä analysoi sitten RNA:ta sitovia proteiineja ja havaitsi, että PTBP1-geeni säätelee kasvaimia edistävää RNA:n silmukointia glioomasoluissa. Käyttämällä ortotooppista glioomamallia immuunipuutteisilla hiirillä tutkijat kohdistivat PTBP1:een antisense-oligonukleotidipohjaisen (ASO) hoidon, joka lopulta esti kasvaimen kasvua.
"Tietomme korostavat vaihtoehtoisen RNA:n silmukoinnin roolia glioomien pahanlaatuisuuden ja heterogeenisyyden vaikuttamisessa sekä sen potentiaalia terapeuttisena haavoittuvuutena aikuisten glioomien hoidossa", tutkimuksen tekijät kirjoittavat.
Tutkijoiden seuraava askel on tutkia PTBP1:n kohdentamisen potentiaalia kasvaimen vastaisen immuunivasteen aikaansaamiseksi, Song sanoi.
"Pitkän lukuajan RNA-sekvensointianalyysin avulla havaitsimme, että PTBP1:n kohdentaminen glioomasoluissa johtaa useiden vaihtoehtoisesti silmukoituneiden transkriptien tuotantoon, joita ei esiinny normaaleissa kudoksissa. Seuraava projektimme on siis selvittää, voiko tämä isoformi tuottaa antigeenejä, jotta immuunijärjestelmä voi paremmin tunnistaa kasvaimen", Song sanoi.
Song lisäsi myös, että heidän tiiminsä on kiinnostunut analysoimaan glioomapotilaiden ei-kasvainsolujen, kuten immuunisolujen, silmukointimuutoksia.
"Tiedämme jo, että silmukointi on erittäin tärkeää solun toiminnan säätelyssä, joten sen pitäisi paitsi säädellä kasvaimen pahanlaatuisuutta, myös immuunisolujen toimintaa sen määrittämiseksi, pystyvätkö ne tehokkaasti tappamaan syövän. Joten teemme myös bioinformatiikan analyysejä kasvaimeen tunkeutuneissa immuunisoluissa nähdäksemme, onko silmukoinnissa muutosta sen jälkeen, kun immuunisolu on tunkeutunut kasvaimeen."
"Tavoitteenamme on selvittää vaihtoehtoisen silmukoinnin rooli immuunisuppressiivisen kasvaimen mikroympäristön muokkaamisessa ja tunnistaa potentiaalisia kohteita immunoterapioiden tehokkuuden parantamiseksi glioomassa", Song sanoi.
