
Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Subkondraalisen luun muutosten merkitys nivelrikon patogeneesissä
Lääketieteen asiantuntija
Viimeksi tarkistettu: 04.07.2025
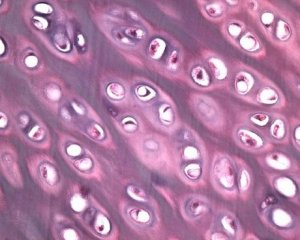
Nivelruston rappeutumisen ohella myös alla oleva luukudos on osallisena nivelrikon patologisessa prosessissa. Oletetaan, että subkondraalisen levyn paksuuntuminen myötävaikuttaa nivelrikon etenemiseen. Nivelrikon edetessä mekaaniselle ja kemialliselle rasitukselle altis nivelrusto kuluu hitaasti ruston katabolian ja korjautumisen prosessien epätasapainon vuoksi. Erityisesti mekaaninen rasitus niveliin, jotka "kannattavat" kehon painoa, myötävaikuttaa suuren määrän mikromurtumien muodostumiseen subkondraalisessa levyssä ja rustossa. Nivelruston kulumisen ja subkondraalisen luun skleroosin edetessä luukudoksen jäykkyys lisääntyy, mikä puolestaan edistää nivelruston rakenteen häiriintymistä entisestään. Kysymys subkondraalisen luun muutosten primaarisesta vai sekundaarisesta luonteesta nivelrikossa on kuitenkin edelleen ratkaisematta.
Vielä äskettäin röntgenkuvissa havaittavia muutoksia subkondraalisen luun sienimäisessä aineessa, kuten skleroosia tai kystan muodostumista, pidettiin toissijaisina nivelrikkopotilailla . Kliinisten ja kokeellisten tutkimusten tulokset kuitenkin viittaavat subkondraalisen luun mahdolliseen aloittavaan rooliin nivelrikon patogeneesissä. Yksi mahdollisista mekanismeista on subkondraalisen luun jäykkyysgradientin jyrkkä nousu, koska alla olevan rustokudoksen eheys riippuu sen luu"pedin" mekaanisista ominaisuuksista. Kädellisillä tehdyt tutkimukset ovat osoittaneet, että subkondraalisen luun muutokset voivat edeltää nivelruston muutoksia. Eläinmallien ja kliinisten tutkimusten tuloksena syntyneet todisteet tätä hypoteesia vastaan ja sitä vastaan ovat vain kiihdyttäneet keskustelua. Subkondraalin luun trabekuloiden paksuuntuminen ei aina liity luun mineralisaation lisääntymiseen tai pikemminkin osteoidin tilavuuden kasvuun. Tämä merkki epänormaalista mineralisaatiosta osoittaa, että luun uudelleenmuodostumisen säätelyn häiriö on olennainen osa nivelrikkoa ja tukee myös luusoluvirheen käsitettä nivelrikossa. J. Dequekerin ryhmä (1989) pitää jälkimmäistä "yleisenä metabolisena luusairautena".
Luukudos uusiutuu jatkuvasti. Tätä dynaamista prosessia, jota kutsutaan luun uudelleenmuodostukseksi, kutsutaan luukudoksen uudelleenmuodostukseksi, ja se on monimutkainen resorption ja mineralisaation sarja. Osteoklastit resorboivat luukudosta, ja osteoblastit erittävät proteiineja, jotka muodostavat mineralisaation pääkomponentin. Luun muodostuminen ja resorptio eivät tapahdu satunnaisesti koko luustossa; se on ohjelmoitu prosessi, joka tapahtuu luuston eri alueilla, joita kutsutaan luun uudelleenmuodostusyksiköiksi. Syklin alkuvaiheessa osteoklastit ilmestyvät inaktiiviselle pinnalle; kahden viikon kuluessa ne muodostavat tunnelin kortikaaliseen luuhun tai aukon trabekulaarisen luun pinnalle. Uusien luun uudelleenmuodostusyksiköiden aktivaatiotiheys määrää luun uusiutumisasteen. Terveellä nuorella ihmisellä luun muodostumis- ja resorptioprosessit ovat tasapainossa ja normaali luumassa säilyy. Luukudosten resorption hormonaaliseen säätelyyn osallistuvat ainakin PTH ja PGE2 , osteoklastien lisäksi myös osteoblastit, koska näiden hormonien vaikutuksesta vapautuu tekijöitä, jotka stimuloivat osteoklastien luun resorptiota. Tällä hetkellä tunnetaan yli 12 paikallista ja systeemistä luukudoksen kasvun säätelijää, jotka vaikuttavat sen uudelleenmuotoutumiseen, erityisesti PTH, 1,25(OH)2D3 ,kalsitoniini, kasvuhormoni, glukokortikoidit, kilpirauhashormonit, insuliini, IGF (1 ja 2), estrogeenit, PGE2 ja androgeenit.
Luusolut vapauttavat useita proteiineja ja sytokiineja, jotka suorittavat hormonaalista säätelyä ja signaalinvälitystä. Osteoblastien tuottamiin proteiineihin kuuluvat luumatriisiproteiinit, kuten kollageeni, osteopontiini, osteokalsiini ja luun sialoproteiinit. Lisäksi nämä solut vapauttavat sekä aktiivisessa että piilevässä muodossa olevia proteaaseja, jotka osallistuvat luukudoksen uudelleenmuodostumiseen - MMP:itä, jotka ovat plasminogeeniaktivaattorin (PA)/plasmiinijärjestelmän komponentteja. Osteoblastien vapauttamat sytokiinit voivat vaikuttaa sekä autokriinisten mekanismien että parakriinisten reittien kautta paikallisiin soluihin (muihin osteoblasteihin, osteoklasteihin).
Ei vielä tiedetä, säätelevätkö mekaaninen rasitus näitä signaaleja vai muut mekaanisen rasituksen aiheuttamat kemialliset signaalit. On kuitenkin tunnettua, että toistuva mekaaninen rasitus aiheuttaa luusolujen ja/tai proteiinien paikallista lisääntymistä. In vivo mekaaninen kuormitus voi aktivoida osteoblasteja, lisätä syklisten nukleotidien määrää, prostaglandiinien tuotantoa ja aiheuttaa luun uudelleenmuodostukseen liittyviä morfologisia muutoksia. In vitro mekaaninen rasitus aiheuttaa osteoblastiviljelmien lisääntymistä, osteoidien muodostumiseen ja mineralisaatioon osallistuvien luuproteiinien mRNA:n ilmentymistä, paikallisten kasvutekijöiden, kuten IGF-1:n ja IGF-2:n, sekä adheesiomolekyylien vapautumista. Mekaanisen rasituksen signaalin välittyminen voidaan suorittaa mekaanisensitiivisten ionikanavien kautta.
Nivelrikossa on epäsuoria todisteita osteoblastien toimintahäiriöistä. G. Gevers ja J. Dequeker (1987) osoittivat seerumin osteokalsiinipitoisuuksien nousua käden nivelrikosta kärsivillä naisilla sekä kortikaalisissa luusiirteissä, mikä viittaa siihen, että luupatologia voi olla osa nivelrikoa. Ruumiinavauksessa havaittiin paitsi subkondraalisen luun paksuuntumista, myös reisiluun pään epänormaalin alhainen mineralisaatio. Marsuilla, joilla oli kirurgisesti aiheutettu nivelriko, tietokonetomografia paljasti merkittävää luufraktion paksuuntumista subkondraalisella alueella. Kollageenin ja ei-kollageenisten proteiinien (osteokalsiini jne.) välinen epätasapaino voi johtaa luun tilavuuden kasvuun, mutta se ei vaikuta sen mineraalitiheyteen. M. Shimizun ym. (1993) mukaan nivelruston degeneratiivisten muutosten eteneminen liittyy subkondraalisen luun voimakkaampaan uudelleenmuotoutumiseen ja sen jäykkyyden lisääntymiseen, mikä myös viittaa luukudossolujen vikaan nivelrikossa. B. Leen ja M. Aspdenin (1997) ehdottaman hypoteesin mukaan viallisten luusolujen lisääntyminen voi johtaa luukudoksen jäykkyyden lisääntymiseen, mutta se ei aiheuta sen mineraalitiheyden kasvua.
CI Westacott ym. (1997) olettivat, että poikkeavat osteoblastit vaikuttavat suoraan ruston aineenvaihduntaan. Viljellessään nivelrikkopotilaiden osteoblasteja nivelsairauksia sairastamattomien ihmisten kondrosyyteillä, kirjoittajat havaitsivat merkittävän muutoksen normaalin rustokudoksen glykosaminoglykaanien vapautumisessa in vitro, mutta sytokiinien vapautumisen taso pysyi muuttumattomana. G. Hilal ym. (1998) osoittivat, että nivelrikkopotilaiden subkondraaliluun osteoblastien viljely in vitro havaittaa muuttuneen aineenvaihdunnan - AP/plasmiinijärjestelmän aktiivisuus ja IGF-1:n taso näissä soluissa lisääntyvät. CI Westacott ym. (1997) havainto voidaan selittää proteaasien aktiivisuuden lisääntymisellä subkondraaliluun soluissa.
On edelleen epäselvää, käynnistävätkö subkondraallisen luun muutokset nivelrikon vai vaikuttavatko ne sen etenemiseen. DK Dedrick ym. (1993) osoittivat, että kirurgisesti aiheutetusta nivelrikosta kärsivillä koirilla subkondraallisen luun paksuuntuminen ei ole välttämätön edellytys nivelrikon kaltaisten muutosten kehittymiselle nivelrustossa, mutta se edistää degeneratiivisten prosessien etenemistä rustossa. A. Sa'ied ym. (1997) tutkimuksen tulokset ovat ristiriidassa aiemman tutkimuksen tietojen kanssa. Käyttämällä 50 MHz:n kaikukuvausta arvioidakseen alkuperäisiä morfologisia muutoksia ja niiden etenemistä nivelrustossa ja luussa kokeellisessa nivelrikossa, joka aiheutettiin monojodietikkahapon injektioilla rottien polviniveleen, kirjoittajat osoittivat samanaikaisen luun ja ruston muutosprosessin kolmen ensimmäisen päivän aikana injektion jälkeen.
Osteoblastit erittävät kasvutekijöitä ja sytokiineja, jotka osallistuvat paikalliseen luun uudelleenmuodostukseen. Nämä voivat edistää ruston uudelleenmuodostusta "painoa kantavissa" nivelissä sen jälkeen, kun ne ovat tunkeutuneet nivelruston kalkkeutuneen kerroksen mikrohalkeamien läpi. Lisäksi luusolujen eritystuotteita löytyy nivelnesteestä. Todennäköisimmät epänormaalien osteoblastien erittämät tuotteet, jotka voivat käynnistää paikallisen ruston uudelleenmuodostuksen, ovat TGF-b ja luun morfometriset proteiinit (BMP). Molempia TGF-perheen jäseniä erittävät sekä kondrosyytit että osteoblastit, ja molemmat kykenevät modifioimaan sekä luun että ruston uudelleenmuodostusta. J. Martel Pelletier ym. (1997) havaitsivat TGF-β:n tason nousun nivelrikkopotilaiden subkondraalisissa luukudoksissa verrattuna terveisiin yksilöihin, mikä viittaa tämän kasvutekijän todennäköiseen rooliin nivelrikon patogeneesissä. Myös osteoblastit tuottavat IGF:itä. Nivelrikkopotilaista saatujen osteoblastien kaltaisten solujen viljelmässä havaittiin IGF:ien tason nousua, mikä muuttaa ruston aineenvaihduntaa.
Subkondraalisessa luussa osteoblastien tuottamat TGF-b, IGF, BMP ja sytokiinit voivat vaikuttaa kollagenaasin ja muiden proteolyyttisten entsyymien tuotantoon rustossa, mikä puolestaan voi edistää rustomatriisin uudelleenmuodostumista/hajoamista. On edelleen epäselvää, tuottavatko nivelrikkoa sairastavat osteoblastit vähemmän makrofagien pesäkkeitä stimuloivaa tekijää (M-CSF - luun resorptiota stimuloiva tekijä) kuin normaalit solut. AG Uitterlindenin ym. (1997) tutkimusten tulokset osoittivat, että osteoblastien ilmentämillä D-vitamiinireseptoreilla, jotka säätelevät useiden näiden solujen syntetisoimien tekijöiden ilmentymistä, voi olla tietty rooli osteofyyttien muodostumisessa, mikä osittain selittää osteoblastien roolia tämän taudin patogeneesissä.
Ottaen huomioon edellä mainittujen tutkimusten tulokset, G. Hilal ym. (1998) ja J. Martel-Pelletier ym. (1997) esittivät seuraavan työhypoteesin subkondraalisen luun uudelleenmuodostumisen ja nivelruston välisestä suhteesta nivelrikossa. Nivelrikon patogeneesin varhaisessa tai pitkälle edenneessä vaiheessa luukudoksen uudelleenmuodostumisprosessi subkondraalisessa luussa tehostuu. Samanaikaisesti toistuva kuormitus johtaa paikallisiin mikromurtumiin ja/tai IGF/IGF:tä sitovan proteiinin (IGFBP) järjestelmän epätasapainon ilmenemiseen subkondraalisen luun osteoblastien epänormaalin vasteen vuoksi, mikä edistää sen skleroosia. Jälkimmäinen puolestaan voi edistää varsinaisen ruston mikromurtumien esiintymistä ja sen matriisin vaurioitumista.
Normaaliolosuhteissa tämä vaurio korjaantuu IGF-1:n ja IGF:tä sitovan proteiinin paikallisen synteesin ja vapautumisen kautta, jotka stimuloivat nivelruston ECM:n muodostumista. Samaan aikaan GF-järjestelmä edistää subkondraalisten luusolujen kasvua ja luumatriisin muodostumista. IGF-järjestelmän anabolinen aktiivisuus lisääntyy nivelrikkopotilaiden subkondraalisessa luussa, kun taas AP/plasmiinijärjestelmän (IGF-järjestelmän paikallinen säätelijä) paikallinen aktivaatio nivelrustossa aiheuttaa sen paikallisia muutoksia. Nivelrikon osteoblasteissa IGF-1 häiritsee plasmiinin AP:n säätelyä positiivisen takaisinkytkennän avulla, mikä voi siten hillitä luukudoksen uudelleenmuodostusta, mikä lopulta johtaa subkondraaliseen skleroosiin. Näin ollen luu- ja rustokudoksessa IGF-1:n ja proteaasien paikallinen induktio johtaa toisaalta rustovaurioihin ja toisaalta subkondraalisen luun paksuuntumiseen, mikä puolestaan myötävaikuttaa ruston lisävaurioihin. Subkondraaliseen skleroosiin liittyvä rustovaurion ja sen korjaavien kykyjen välinen epätasapaino johtaa ruston solukalvon (ECM) etenemiseen ja nivelrikon kehittymiseen. Kirjoittajien mukaan tämä hypoteesi selittää myös taudin hitaan etenemisen.

